Evaluación de la función diastólica del VI. Guías y recomendaciones de la sociedad Británica de Ecocardiografia.
- cyntia machain leyva
- 17 jun 2024
- 30 Min. de lectura
Robinson et al. Echo Research & Practice (2024) 11:16
El deterioro de la función diastólica del ventrículo izquierdo (VI) es común entre aquellos con enfermedad del corazón izquierdo y se asocia con una morbilidad significativa. Dado que, en términos simples, el ventrículo sólo puede expulsar el volumen con el que se llena y que aproximadamente la mitad de las hospitalizaciones por insuficiencia cardíaca (IC) corresponden a personas con fracción de eyección del ventrículo izquierdo normal o preservada (HFpEF). Cuando las anomalías del llenado ventricular son la causa de los síntomas, está claro que la evaluación de la función diastólica del ventrículo izquierdo (DFVI) es crucial para comprender la función cardíaca global y para identificar los efectos más amplios de los procesos patológicos. Los métodos invasivos para medir la relajación y las presiones de llenado del VI se consideran el estándar de oro para investigar la función diastólica. Sin embargo, la alta resolución temporal de la ecocardiografía transtorácica (ETT) con medidas ampliamente validadas y reproducibles disponibles al lado de la cama del paciente y sin la necesidad de procedimientos invasivos que involucran radiación ionizante han establecido a la ecocardiografía como la modalidad de imagen primaria.
La evaluación integral de función diastólica del VI es, por tanto, un elemento fundamental de la realización del ETT. Sin embargo, la evaluación ecocardiográfica de la función diastólica es compleja. En los términos más amplios y básicos, la diástole ventricular comprende una fase de llenado temprana en la que la sangre se extrae, mediante succión, hacia el ventrículo a medida que retrocede y se alarga rápidamente la contracción sistólica precedente y el acortamiento. A esto le sigue en la diástole tardía la distensión del VI distensible, cuando la contracción auricular contribuye activamente al llenado ventricular. Cuando la función diastólica es normal, el llenado ventricular se logra a baja presión tanto en reposo como durante el esfuerzo. Sin embargo, esta descripción básica simplemente resume la compleja fisiología que permite el proceso diastólico y lo define según el método mecánico mediante el cual se llenan los ventrículos, pasando por alto la función miocárdica, las propiedades de distensibilidad de la cámara y los diferenciales de presión que determinan la capacidad de Llenado del VI. A diferencia de la función sistólica ventricular, donde se utilizan parámetros únicos para definir el rendimiento miocárdico (fracción de eyección del VI (FEVI) y deformación longitudinal global (SLG)), la evaluación de la función diastólica se basa en la interpretación de múltiples parámetros de velocidad del miocardio y del flujo sanguíneo, junto con tamaño y función de la aurícula izquierda (AI), para diagnosticar la presencia y el grado de deterioro. Por lo tanto, la evaluación ecocardiográfica de la función diastólica es multifacética y compleja, y requiere un enfoque algorítmico que incorpore medidores de relajación/retroceso del miocardio, distensibilidad y función de la cámara bajo condiciones de carga variables y las presiones intracavitarias bajo las cuales ocurren estos procesos. Esta guía describe un enfoque estructurado
de la evaluación de la función diastólica e incluye recomendaciones para la evaluación de la relajación del VI y las presiones de llenado. Las medidas ecocardiográficas no rutinarias se describen junto con pautas para su aplicación en circunstancias específicas. Se describen métodos provocativos para revelar una mayor presión de llenado durante el esfuerzo y se consideran modalidades novedosas y emergentes.
MECANICA, FISIOLOGIA Y ANATOMIA VENTRICULAR.
-Alineación de miocitos que define las capas miocárdicas.
Es el acortamiento y alargamiento de los miocitos cardíacos a lo largo de planos de alineación lo que permite que la cavidad ventricular disminuya y aumente de volumen, produciendo la eyección sistólica y el llenado diastólico. La mayor parte del miocardio ventricular está compuesta de miocitos contráctiles que se ramifican en cada extremo para formar conexiones con miocitos adyacentes. Esta conectividad de ramas crea una red interconectada de cardiomiocitos que forma la base de la arquitectura de múltiples capas del miocardio ventricular, permitiendo los complejos procesos de contracción y relajación ventricular. Cuando se considera según la alineación y orientación de los miocitos, el miocardio del VI consta de tres capas, aunque sin límites distintos entre ellas: el subepicardio, la pared media y el subendocardio. Las fibras subepicárdicas están orientadas en una disposición helicoidal izquierda (LH) y representan alrededor del 25% del espesor total de la pared del miocardio. Alineados oblicuamente longitudinales, se extienden desde el nivel de las válvulas auriculoventriculares en la base de los ventrículos. Cuando se ven desde una perspectiva anterior, las fibras subepicárdicas discurren oblicuamente hacia la izquierda y continúan hasta el ápice; las fibras que se originan en la base del ventrículo izquierdo se extienden hacia la superficie diafragmática del corazón, cruzando el surco interventricular posterior. La contracción de esta capa es en gran medida responsable de la torsión del ápice con respecto a la base. Las fibras de la pared media representan alrededor del 53-59% del espesor del miocardio, aumentando en los ancianos, y están dispuestas circunferencialmente y en alineación casi paralela con el anillo de la válvula mitral (VM); estas fibras generan en gran medida contracción radial. La capa subendocárdica es la capa más delgada y representa <20% del espesor total del miocardio. Estas fibras
están dispuestos en una hélice derecha (RH) y un patrón longitudinal oblicuo, generando una contracción longitudinal y rotacional de esta capa. Fundamentalmente, el VI consta de dos hélices musculares que rodean la capa circunferencial media del ventrículo de fibras musculares.
-Mecanica miocardica y contracción Ventricular.
Esta configuración compleja de alineación de los miocitos (subepicárdica: hélice mano izq, subendocárdica: hélice mano der, pared media: circunferencial) permite la contracción tridimensional que da como resultado la rotación, el acortamiento y la contracción hacia adentro del miocardio con el efecto neto de reducir Dimensiones de la cavidad del VI en todos los planos.
La contracción de las fibras subepicárdicas, dispuestas en una hélice LH, provoca la rotación en sentido antihorario del subepicardio apical y la rotación de la base en el sentido de las agujas del reloj, mientras que la contracción de las fibras subendocárdicas, dispuestas en una hélice RH, provoca la rotación en el sentido de las agujas del reloj del subendocardio apical y la rotación en el sentido contrario a las agujas del reloj en la base (Fig. 1). Sin embargo, debido a que el radio de rotación de la capa externa es mayor que el de la capa interna y, por lo tanto, produce un mayor torque, la dirección de contracción subepicárdica domina cuando ambas capas se contraen simultáneamente. En consecuencia, la rotación apical global es en el sentido de las agujas del reloj muy brevemente durante la contracción isovolumétrica antes de invertirse y girar en el sentido contrario a las agujas del reloj durante la fase de eyección (Fig. 2). La contracción basal global refleja este proceso, girando en sentido antihorario muy brevemente durante la contracción isovolumétrica antes de invertir la rotación en el sentido de las agujas del reloj durante la eyección sistólica. Por lo tanto, la rotación sistólica global del VI es predominantemente en sentido antihorario en el vértice y en el sentido de las agujas del reloj en la base (Fig. 3).
Desde una perspectiva mecanica, la torsión del miocardio a lo largo de estos planos ayuda a mantener una posición uniforme del estrés y acortamiento de las fibras miocárdicas que produce un alto porcentaje de contracción global (FEVI ~60%) a partir de un acortamiento de miocitos relativamente pequeño (~20%). Es importante destacar que para la eficiencia del llenado diastólico, la torsión y deformación de la matriz miocárdica a lo largo de la sístole provoca una acumulación progresiva de energía potencial. Esta energía se libera después de la contracción máxima resultando en un rápido retroceso de las fibras circunferenciales y desenroscamiento de las hélices subepi y subendocárdica durante la relajación isovolumétrica y el período inicial de llenado diastólico. El desenroscamiento del ápice en el sentido de las agujas del reloj y el desenroscamiento simultáneo de la base en el sentido contrario a las agujas del reloj genera una relajación rápida de la cavidad del VI y, en consecuencia, una succión diastólica temprana.
Debido a la naturaleza tomográfica de la ETT 2D de rutina, esta contracción tridimensional compleja se ve y, por lo tanto, se mide en planos ortogonales 2D: el Doppler tisular del anular mitral (TDI) y el SLG miden el alargamiento/acortamiento longitudinal del VI, mientras que la FEVI mide predominantemente la contractilidad radial con una contribución menor del acortamiento longitudinal. Por lo tanto, debido a que la contracción y relajación de los cardiomiocitos no es puramente longitudinal o radial en dirección, los índices 2D de deformación en estos planos no reflejan precisamente la contracción del miocardio del VI. No obstante, estas medidas ecocardiográficas de la contracción longitudinal y radial están bien validadas y proporcionan información diagnóstica y pronóstica importante sobre los procesos patológicos y su efecto sobre la función miocárdica.
-Función ventricular izquierda normal durante todo el ciclo cardíaco.
El ciclo cardíaco del VI se divide en términos generales en dos fases: sístole y diástole. Aunque estas fases a menudo se consideran de forma independiente cuando se investigan mediante ecocardiografía, la capacidad del ventrículo para llenarse y expulsarse refleja el rendimiento miocárdico global. Dado que el grado de contracción sistólica y eyección debe ser igual al de relajación y llenado diastólico (ya que el ventrículo no puede expulsar perpetuamente más volumen del que ha entrado en la cámara durante el período de llenado anterior, y viceversa), existe una interdependencia crucial. entre la función sistólica y diastólica del VI. En consecuencia, ambas fases son simultáneamente susceptibles al deterioro secundario a procesos patológicos y aunque la disfunción de una fase puede ser la causa predominante de los síntomas, es muy probable que esto vaya acompañado por algún grado de deterioro del otro. Por lo tanto, para comprender completamente los mecanismos fisiológicos que gobiernan los tiempos y los diferenciales de presión que permiten el llenado ventricular, y para apreciar la importancia de la interdependencia sistólica/diastólica, es esencial comprender la función ventricular a lo largo del ciclo cardíaco y cómo esto determina el llenado, la presión de llenado (LVFP) y la expulsión.
-Sístole ventricular izquierda
La sístole del VI se define como el período entre el cierre de la VM y el cierre de la válvula aórtica (AV) y consta de dos fases que se denominan según los cambios de volumen del VI: contracción isovolumétrica y fase de eyección.
-Contracción isovolumétrica
La diástole y el llenado del VI terminan cuando se completa la contracción de la AI y las presiones LA-VI son casi iguales, lo que lleva al inicio del cierre de la VM (Fig. 4). Con el inicio de la contracción sistólica, la presión de la cavidad del VI aumenta por encima de la presión de la AI (LAP) y el VM se cierra. Aunque la presión del VI aumenta y excede la LAP, permanece por debajo de la presión dentro de la aorta y la VAo permanece cerrada. Por lo tanto, debido a que el ventrículo está dentro de la fase contráctil pero la presión interna impide que la sangre entre o salga de la cámara, este período se denomina tiempo de contracción isovolumétrica (IVCT).
-Eyección sistólica
Una vez que la presión del VI excede la presión aórtica, el VAo se abre y la sangre se expulsa del VI; este período se conoce como fase de expulsión. Aunque la contracción y deformación sistólica máxima se alcanza en la sístole tardía, la presión máxima del VI y, en consecuencia, las velocidades de salida, alcanzan su punto máximo en la sístole media antes de caer a medida que el volumen ventricular disminuye hacia el final de la sístole. El VAo se cierra después de la contracción máxima del VI cuando la presión de la cavidad cae por debajo de la presión en la aorta, lo que define el final del período sistólico.
-Diástole del ventrículo izquierdo
La diástole se define como el período entre el cierre VAo y el cierre VM e incluye períodos de relajación isovolumétrica y llenado ventricular. En ritmo sinusal (SR) con frecuencia cardíaca (FC) normal y sin retraso de conducción entre las aurículas y los ventrículos, la diástole es un proceso de cuatro fases que comprende períodos de: relajación isovolumétrica, llenado rápido temprano, un período de poco o ningún llenado ( diástasis) y contracción auricular (Fig. 4).
-Relajación isovolumétrica
A lo largo de la sístole, la compresión y torsión del miocardio genera una acumulación progresiva de energía potencial dentro de los elementos elásticos de los cardiomiocitos y la matriz extracelular, alcanzando su punto máximo al final de la sístole. Luego, esta energía se libera en la diástole temprana cuando los cardiomiocitos retorcidos y comprimidos retroceden y se relajan hasta su orientación sin estrés/reposo, lo que resulta en un rápido retroceso y desenrosque del VI. Combinado con una contribución de la relajación activa de los miocitos, esto conduce a un rápido aumento en las dimensiones de la cavidad del VI que causa una caída igualmente rápida en la presión intracavitaria. Esta tasa casi constante de relajación del VI provoca una tasa casi exponencial de caída de presión que puede medirse mediante la constante de tiempo, Tau (τ). Dado que la velocidad a la que cae la presión intracavitaria está determinada por τ, la velocidad de caída de la presión puede medirse como un indicador de la relajación del VI y, por lo tanto, de la función miocárdica diastólica.
El inicio de la diástole se define mecánicamente por el cierre de la VAo. Por lo tanto, la presión del VI al inicio de la diástole es alta y justo por debajo de la presión aórtica (Fig. 5). Durante un breve período después del cierre VAo, a pesar de caer, la presión dentro del VI que se relaja rápidamente continúa excediendo la LAP y el VI permanece cerrado sin, en consecuencia, ningún llenado ventricular. Dado que tanto VAo como VM están cerrados y el volumen del VI no cambia desde el punto de cierre VAo, esta fase se describe como Tiempo de Relajación Isovolumétrica (TRIVI) (Fig. 5) y dura entre el cierre VAo y la apertura de VM. . Tanto en el estado normal como en el de enfermedad, la tasa de relajación es constante con una relación casi lineal con τ; Debido a que una τ normal suele ser inferior a 45 ms en la mayoría de los grupos de edad, la TRIV es corta en aquellos con función diastólica normal.
-Llenado temprano
La continua destorsión y relajación del VI hace que la presión intracavitaria disminuya. Una vez que la presión en el VI cae por debajo de la presión en la AI, el efecto de succión hace que el VI se abra y la sangre fluya desde la AI hacia el VI, lo que marca el inicio de la fase de llenado rápido temprano y el final de la IVRT (Fig. 6). Durante un período muy breve de 30 a 40 ms después de la apertura del VM, la rápida tasa de relajación del VI es tal que la presión dentro del VI continúa cayendo a pesar del aumento inicial de volumen, lo que crea un gradiente de presión desde la AI hasta el vértice del VI que da como resultado una aceleración del flujo fuera de la AI; Por tanto, la presión diastólica mínima del VI se alcanza normalmente en torno a 3,5×τ. Con una relajación continua del VI y un volumen del VI que aumenta rápidamente hacia su capacidad relajada, la presión en la cavidad del VI aumenta con una reducción progresiva en la diferencia de presión LA-VI y la consiguiente caída en la velocidad del flujo transmitral. En corazones jóvenes sanos y con una frecuencia cardíaca normal, entre el 80 y el 90% del llenado total del VI se produce durante la fase de llenado diastólico temprano y la mayor parte del llenado temprano del VI se completa en 140 ms.
-Diástasis
A medida que finaliza el período de llenado temprano y el VI alcanza su volumen relajado, las presiones diastólicas del VI aumentan con poca o ninguna diferencia de presión entre la AI y el VI. En consecuencia, el volumen y la velocidad del flujo transmitral caen significativamente y las valvas MV vuelven a una posición semiabierta o incluso casi cerrada. Este período de poco o ningún flujo después del llenado pasivo temprano y antes de la contracción auricular se denomina diástasis. Con un intervalo P-R normal, la duración de la diástasis está determinada por el período diastólico y, por tanto, la FC, y la bradicardia produce un período más largo entre la fase de llenado temprana y la contracción auricular y, por tanto, una diástasis más prolongada.
-Llenado tardío por contracción auricular
La fase final del llenado ventricular ocurre cuando la contracción de la AI aumenta la presión de la AI, lo que obliga al VI a abrirse y expulsar sangre hacia el VI. En el contexto de una función diastólica normal, el VI relajado ofrece muy poca resistencia al llenado adicional y la mayor parte de la sangre expulsada por la AI ingresa al VI, y sólo una pequeña proporción se expulsa de regreso a las venas pulmonares. Durante esta etapa final de la diástole, debido a que los cardiomiocitos del VI están completamente relajados, altamente distendibles y distensibles, el volumen adicional del 10 al 20% procedente de la contracción auricular se logra con un aumento de < 5 mmHg en la presión diastolica final. Esto permite que el VI se llene a una presión muy baja, en consecuencia, una presión baja dentro de la AI, las venas pulmonares (PV) y, por lo tanto, el lecho capilar pulmonar (Fig. 6).
Función auricular y flujo de las venas pulmonares.
Como reservorio de sangre antes del llenado diastólico temprano del VI y a través de la contribución de la bomba en la diástole tardía, la función de la AI modula el llenado del VI y, por lo tanto, es un componente importante de la función diastólica del VI. En relación con la AI, el flujo de las VPs refleja las fases de llenado y contracción de la AI y, por lo tanto, proporciona información sobre LVDF, LVFP y LAP. En la RS, hay tres fases de la función de la AI, cada una de las cuales es identificable durante la ETT por alteraciones en las dimensiones de la cámara de la AI y por el flujo sanguíneo que entra y sale de la AI (Fig. 7).
-Fase de reservorio.
La fase de reservorio de AI ocurre durante la contracción sistólica del VI y el flujo de PV durante este período ocurre en dos fases. Al comienzo de la sístole del VI, el retroceso elástico de la AI inmediatamente después de la contracción auricular hace que las dimensiones aumenten y la presión de AI disminuya, extrayendo sangre de las VP y marcando la fase inicial del flujo sistólico de las VP. La contracción sistólica continua y el acortamiento del VI conducen al descenso del anillo del VI hacia el vértice del VI. Como el techo de la AI tiene una posición relativamente fija, este movimiento estira la AI y aumenta las dimensiones desde un mínimo contraído al final de la diástole hasta un volumen máximo en el final de la sístole ventricular (Fig. 7).
El aumento de las dimensiones de la AI hace que la presión de la AI caiga aún más mientras que la presión sistólica del ventrículo derecho (VD) se propaga simultáneamente a través de la vasculatura pulmonar. Estas acciones se combinan para crear una diferencia de presión que impulsa el flujo sanguíneo a través de los pulmones y las VP hacia la AI, lo que se conoce como la segunda fase del flujo de VP (Fig. 8). Por tanto, la AI funciona como un "depósito" de sangre durante la sístole del VI. Como el llenado de la AI durante esta fase depende de una combinación de estiramiento de la cámara (a través del acortamiento longitudinal del VI), presión sistólica del VD propagada a través de los pulmones y distensibilidad intrínseca de la AI, este aspecto de la función de la AI está ampliamente relacionado con el volumen sistólico (VS) del VI. y distensibilidad auricular.
-Fase de conducto
La fase del conducto AI comienza con la apertura de la VM y continúa hasta la contracción auricular activa. Sin embargo, en la fibrilación auricular (FA), la ausencia de contracción auricular hace que esta fase continúe hasta el final de la diástole. La fase de conducto está representada por el volumen de sangre que se transporta desde las PV al VI sin almacenarse en la aurícula y puede estimarse considerando los cambios en las dimensiones de la AI en comparación con el SV del VI, de la siguiente manera:
En circunstancias normales (ausencia de insuficiencia aórtica o mitral), el volumen de sangre eyectada por el VI en sístole, el SV, es igual al volumen de sangre que llena en diástole (volumen de llenado total). Este volumen de llenado diastólico total (y por lo tanto SV) se logra mediante dos mecanismos de llenado que ocurren simultáneamente:
a) vaciado de la AI desde su volumen máximo al final de la sístole hasta un volumen mínimo después de la contracción auricular al final de la diástole: volumen del reservorio de la AI.
b) sangre aspirada hacia el VI por efecto de succión, secundaria a la relajación del VI al principio y a la mitad de la diástole, que simplemente pasa a través de la AI desde el volumen del conducto PV-LA.
La contribución del volumen de reservorio de AI al llenado del VI se calcula como la diferencia entre el volumen máximo de AI y el volumen mínimo de AI. Por lo tanto, debido a que el volumen total de llenado del VI y el volumen latido son iguales, la contribución del volumen del conducto al llenado del VI se calcula como la diferencia entre el volumen del reservorio de AI y el volumen latido
-Fase de contracción activa
La etapa final de la función de la AI es la fase de bombeo, a veces descrita como fase contráctil, cuando la sangre se expulsa activamente hacia el VI. La contracción de la AI contribuye entre el 10 y el 15 % del llenado total en los jóvenes sanos, aumentando hasta el 35-40 % en los ancianos sanos. Cuando la presión diastolica del VI es normal, la mayor parte de la sangre expulsada de la AI ingresa al VI y se identifica como la onda A en el Doppler transmitral. Sin embargo, incluso en corazones normales y sanos, la contracción de la AI produce la expulsión de un pequeño volumen de sangre hacia las venas pulmonares (Fig. 8). La fase de bombeo de AI es un mecanismo importante mediante el cual se puede maximizar el llenado del VI y mantener el volumen latido.
El espectro de la función diastólica alterada.
Aunque los eventos cardíacos repentinos pueden tener un efecto adverso inmediato sobre la función diastólica del VI y la presión final del VI, el desarrollo de una función diastólica alterada suele ser un proceso crónico en el que el deterioro suele estar determinado por la etiología y la eficacia del tratamiento médico de la enfermedad subyacente. Muchos procesos patológicos afectan la función miocárdica y, en consecuencia, alteran las propiedades de relajación y distensibilidad del ventrículo izquierdo, limitando así la capacidad de llenado del VI y provocando que aumenten las presiones diastólicas del VI y la AI. Aunque la función diastólica alterada describe ampliamente el complejo continuo desde la normalidad hasta el llenado restrictivo, tres aspectos fisiológicos importantes definen la capacidad de llenado del VI y deben ser considerados mediante ecocardiografía: relajación miocárdica, distensibilidad de la cámara y LVFP. Si bien no hay certeza de la progresión, la función diastólica alterada se presentará inicialmente en las primeras etapas como una anomalía subclínica de la relajación sin ningún efecto significativo sobre la presión final del VI o los síntomas asociados. Si es progresiva, puede avanzar a través del espectro de deterioro hasta un llenado ventricular restrictivo con las consecuencias hemodinámicas significativas de una presión diastolica final del VI marcadamente elevada y una hipertensión pulmonar (HP) que causan los síntomas de la IC.
Mediciones ecocardiográficas: medidas rutinarias, complementarias y no rutinarias.
Dados los múltiples aspectos de la mecánica diastólica y la presión final del VI asociada, no existe un único parámetro o medida que describa con precisión la función diastólica ventricular y la respuesta de la presión intracavitaria. Por lo tanto, la evaluación ecocardiográfica de la diástole del VI debe incorporar múltiples parámetros de velocidad del flujo sanguíneo intracardíaco, velocidad de relajación miocárdica y tamaño y función de la aurícula izquierda para considerar la presencia y el grado de alteración diastólica. La optimización de todas las imágenes bidimensionales y formas de onda Doppler debe realizarse de acuerdo con las recomendaciones.
-Mediciones de rutina.
1.- Onda E transmitral. La onda E transmitral Doppler representa el llenado temprano del VI debido a una relajación rápida. Aunque la medición del pico E no es una medida directa de presión de AI cuando se aplica la ecuación simplificada de Bernoulli (debido a la resistencia inercial de la sangre dentro de la válvula), la velocidad del pico E está determinada por la diferencia de presión entre LA y VI y por lo tanto refleja LAP. Como tal, la velocidad E puede considerarse junto con otras medidas para la interpretación de la función diastólica y la FEVI. En el corazón joven y sano, la relajación rápida provoca una presión mínima del VI baja que aumenta la diferencia de presión transmitral. Esto crea un efecto de succión en el contexto de presión de AI normal que permite que la mayor parte del llenado ventricular ocurra en la fase diastólica temprana y a alta velocidad, lo que resulta en una velocidad E alta. Con el envejecimiento normal, la desaceleración de la tasa de relajación ventricular hace que el efecto de succión se atenúe, lo que a su vez conduce a una presión mínima más alta, una reducción en el gradiente de presión transmitral diastólica temprana y una caída en la velocidad E transmitral.
2.- Tiempo de desaceleración de la onda E
La desaceleración de la onda E mide el tiempo entre la velocidad máxima del flujo transmitral temprano (pico E) y el punto en el que termina el flujo, o el punto en el que se produce la contracción auricular. El inicio de la desaceleración E mitral corresponde al cruce de presión LA-VI y la inversión del gradiente de presión transmitral que actúa como una fuerza de desaceleración. En pacientes con un ventrículo remodelado y rígido, un gran volumen de llenado temprano, como se refleja en una alta velocidad E, conduce a un rápido aumento de la presión del VI y a un alto gradiente de desaceleración que causa un tiempo de desaceleración E corto. Por lo tanto, el tiempo de desaceleración E es un marcador de rigidez diastólica del VI, aunque en grados más leves de disfunción diastólica el tiempo de desaceleración E está más influenciado por la relajación del VI. En corazones jóvenes sanos, el rápido retroceso y relajación del VI dan como resultado un llenado altamente eficiente y un gran volumen de sangre que ingresa al VI muy rápidamente con la consiguiente rápida igualación de la presión entre la AI y el VI. Por lo tanto, la desaceleración del flujo es igualmente rápida con un corto período de tiempo entre la velocidad máxima E y el final del flujo diastólico temprano, lo que se refleja como una desaceleración de la onda E corta. Sin embargo, a medida que la relajación del VI se ralentiza con el envejecimiento normal, la velocidad y el volumen de llenado del VI disminuyen y se alarga el tiempo de desaceleración de la onda E. Por lo tanto, se espera un tiempo de desaceleración E prolongado en las personas mayores.
3.- Velocidad de onda transmitral A
En RS, el llenado del VI concluye con la contracción auricular en la diástole tardía, representada como la onda transmitral A en la imagen Doppler. Un VI distensible puede aumentar el volumen telediastólico con sólo un pequeño aumento de presión. Con una función diastólica normal, la mayor parte del llenado total del VI se produce en la diástole temprana con una pequeña contribución de la contracción de la AI al llenado general, generalmente del 10 al 20%. Por lo tanto, con una distensibilidad normal del VI, la baja diferencia de presión entre la AI y el VI en la diástole tardía y la baja contribución de volumen de la contracción de la AI dan como resultado una velocidad de onda A transmitral que típicamente es menor que la velocidad de la onda E. En individuos jóvenes, la velocidad A suele ser < 50 cm/s. Sin embargo, la disminución de la relajación del VI relacionada con la edad reduce el llenado diastólico temprano con la consiguiente reducción del vaciamiento de la AI. El vaciado reducido conduce a un aumento en el volumen de la AI (precarga) antes de la contracción en la diástole tardía, lo que resulta en un mayor volumen de bomba de la AI y, por lo tanto, una mayor velocidad de la onda A, a menudo hasta alrededor de 75 cm/s en los ancianos.
4.- Relación E/A
La relación entre las velocidades transmitrales E y A refleja la relación entre el llenado diastólico temprano y tardío del VI. La relajación eficiente en corazones jóvenes sanos permite que la mayor parte del llenado del VI se produzca en la diástole temprana, con una contribución relativamente baja de la contracción auricular y a baja velocidad. Por lo tanto, la relación E/A en individuos jóvenes y sanos suele ser >1. En aquellos que están entrenados atléticamente, una relajación diastólica temprana altamente eficiente puede dar como resultado una relación E/A de hasta 2. El envejecimiento natural conduce a una tasa más lenta de relajación del VI con una reducción en el volumen de llenado diastólico temprano y una caída en la velocidad E, el volumen latido normal se mantiene mediante un aumento en el volumen de llenado de la contracción auricular. Este aumento en el volumen de contracción auricular se refleja en un aumento en la velocidad A que excede la velocidad E y, por lo tanto, un cambio en la relación E/A a < 1.
5.- Imagen Doppler tisular (TDI). Velocidad de la onda e´.
El movimiento del anillo del VI a lo largo del ciclo cardíaco refleja un acortamiento y alargamiento longitudinal tanto del VI como de la AI. En sístole, el VI se acorta, tirando del VI hacia abajo y hacia el ápice del VI, estirando así la AI y aumentando sus dimensiones. Después de la contracción y el acortamiento sistólico máximo, el VI se relaja y se alarga en la diástole temprana, empujando el anillo mitral hacia arriba y acortando/comprimiendo la AI. En la diástole tardía, la contracción auricular provoca un mayor acortamiento de la AI, empujando el anillo de la VM aún más hacia arriba. Por lo tanto, la velocidad fásica del movimiento anular mitral refleja la función miocárdica a lo largo del ciclo cardíaco y puede medirse mediante TDI como un indicador de la contractilidad sistólica y la relajación y distensibilidad diastólica: S′ refleja el acortamiento sistólico del VI, e′ refleja relajación diastolica temprana y a′ que reflejan la contracción auricular en la diástole tardía.
En el corazón sano de personas jóvenes y de mediana edad, las velocidades anulares del VM son altas tanto durante el descenso sistólico como durante el ascenso diastólico, lo que refleja la función dinámica tanto de la AI como del VI. En aquellos que están entrenados atléticamente, la remodelación cardíaca adaptativa conduce a una función cardíaca súper eficiente y un marcado predominio del llenado diastólico temprano, típicamente reflejado por velocidades anulares de la VM sistólica y diastólica temprana que son supranormales. Con el llenado normal del VI, debido a la relajación rápida y eficiente del corazón sano, el inicio del flujo sanguíneo transmitral diastólico temprano ocurre casi simultáneamente con e′. Sin embargo, incluso en el corazón normal se esperan diferencias regionales en las velocidades máximas de relajación. Debido a las diferencias en la extensión del movimiento longitudinal entre las paredes septal y lateral, las velocidades anulares septales suelen ser más bajas en comparación con las de la pared lateral. Como la relación entre la velocidad máxima e′ y τ es inversa, donde una relajación más lenta conduce a un aumento de τ y una disminución de e′, las velocidades de e′ generalmente disminuyen con el envejecimiento normal (Tabla 2).
6.- E/e′
En corazones normales con función diastólica normal y relajación normales, la velocidad e′ está directamente relacionada con el gradiente de presión transmitral y la indexación a la velocidad E para E/e′ no se correlaciona con la presión final del VI. Cuando la presión final del VI es normal pero la tasa de relajación del VI se reduce debido al envejecimiento normal o función diastolica deteriorada, se reducen las velocidades E y e′. Sin embargo, debido a que la reducción tanto en E como en e′ es casi proporcional, la relación entre ellos permanece relativamente sin cambios y <14 en la mayoría de los individuos de todos los grupos de edad. La progresión de la función diastólica deteriorada se caracteriza por un empeoramiento de la relajación del VI, con una mayor reducción de la velocidad e′ y una disminución de la distensibilidad del VI que conduce a una elevación de la presión final del VI y, por lo tanto, a un aumento de la velocidad E. Por lo tanto, un aumento de la relación E/e′ es un marcador de aumento de presion final del VI y la presión de la AI. Un valor < 8 es específico para una presión final del VI normal y un promedio de E/e′ septal y lateral > 14 es altamente específico para una PCWP de > 15 mmHg y, por lo tanto, una presión telediastolica elevada.
7.- Volumen de la AI.
En el corazón sano normal, la AI es una cámara de paredes delgadas que funciona a baja presión, generalmente a una media de alrededor de 8 mmHg. Las dimensiones de la AI están determinadas principalmente por la masa corporal magra del paciente y debido a que el tamaño de la AI no aumenta debido únicamente al envejecimiento, la dilatación de la AI se considera, por lo tanto, un hallazgo anormal en todos los grupos de edad.
Volumen AI: función diastólica alterada
El grado en que la AI se dilata secundariamente a una función diastólica del VI deteriorada está determinada no sólo por la presión AI, sino también por la distensibilidad intrínseca de la AI, el estado general de hidratación/volumen y la distensibilidad de la orejuela auricular izquierda para ayudar a descargar la LAP. Por lo tanto, debido a que la relación entre el volumen y la presión de la AI no es lineal, una presión de la AI específico no se correlaciona directamente con un volumen de AI específico. En consecuencia, la correlación directa entre la presión AI y el volumen de AI no es fuerte. Sin embargo, los volúmenes máximo y mínimo de AI están relacionados con presión de la AI y aumentan en respuesta a la elevación crónica. Por lo tanto, la dilatación de la AI es un hallazgo esperado en aquellos con función diastolica alterada y presiones finales del VI crónicamente elevada.
8.- Velocidad de la regurgitación tricuspidea.
La continuidad entre la AI, las venas pulmonares y el sistema capilar pulmonar hace que la elevación de presión de la AI se transmita a través de la vasculatura pulmonar, lo que lleva a presiones pulmonares elevadas. Por lo tanto, en ausencia de otras causas de HP, la velocidad de la regurgitación tricuspídea (IT) puede considerarse indicativa de la presión de la arteria pulmonar sistólica (PSAP) y, por lo tanto, incorporarse a la evaluación de la función diastolica y la estimación de la presión telediastolica.
9.- Función de la AI: análisis de deformación
Aunque la función auricular se puede evaluar midiendo el volumen de la AI en puntos específicos del ciclo cardíaco, este es un proceso que requiere mucho tiempo y está limitado por una resolución temporal baja (velocidad de fotogramas baja) a frecuencias cardíacas más altas. El análisis de la deformación es considerablemente más rápido y está en gran medida automatizado, por lo que se presta más fácilmente para su uso en medicina clínica. El análisis de la deformación AI proporciona parámetros para todas las fases de la función AI, la fase de reservorio (LAR) y la fase de bombeo (LAP) son importantes para la evaluación de función diastólica.
Se han establecido dos metodologías para la evaluación de la tensión auricular, pero difieren según el punto de referencia cero (es decir, el punto de partida definido del análisis; Fig. 10). La convención para medir la deformación del VI es que el acortamiento relativo de las fibras se asocia con la compresión del miocardio y, por lo tanto, un valor de deformación "negativo", y el alargamiento relativo de las fibras con un valor "positivo". Aunque este sigue siendo el principio para la evaluación de las AI, el punto del ciclo cardíaco en el que comienza la medición determinará el valor de deformación calculado.
En la mayoría de los datos publicados, el QRS se define como el punto de referencia cero y, por tanto, es el método preferido de la BSE. Según el proveedor, el análisis de deformación se puede realizar en una sola vista A4C o en un promedio global por biplano desde las vistas A4 y A2C optimizadas para dimensiones máximas de LA. Al igual que con las estimaciones del volumen máximo de la AI, las vistas A2C y A4C optimizadas para el VI no proporcionan el mayor volumen de la AI y, por lo tanto, sobreestiman los valores de la AI. Los valores de AI no difieren entre hombres y mujeres y se han descrito intervalos de referencia normales tanto en metanálisis como en estudios de corazones sanos normales (Tabla 3).
Deformación de reservorio de la AI: las dimensiones de la AI aumentan desde un mínimo posterior a la contracción al final de la diástole hasta un máximo al final de la sístole. Por lo tanto, la deformación positiva del reservorio refleja el alargamiento total de la AI.
Deformación de la bomba de la AI: las dimensiones de la AI disminuyen a medida que el VI se alarga en la diástole temprana y se reducen aún más las dimensiones de la AI después de la contracción auricular. Por lo tanto, los valores de deformación de la bomba son negativos.
-Deformación LA en la evaluación de la función diastólica del VI
Es bien sabido que las aurículas dilatadas se asocian con un peor pronóstico en una variedad de estados de enfermedades cardiovasculares. Sin embargo, el aumento del volumen de la AI no confirma el aumento de la presión de la AI ni identifica la función de la AI. Por ejemplo, se sabe que la dilatación de la AI ocurre como consecuencia de ciertas condiciones fisiológicas normales, incluido el acondicionamiento atlético y los estados bradicárdicos prolongados. En ambos escenarios, la presión y la función de la AI permanecen normales, lo que sugiere que la función más que el volumen puede ser más relevante al investigar enfermedades que afectan la función diastólica del VI.
Las alteraciones claras y evidentes de la función de la AI en una variedad de enfermedades cardíacas reflejan la sensibilidad y utilidad del strain AI para la evaluación de la función diastólica del VI alterada. La medición de LAVi se ha considerado durante mucho tiempo crucial para la evaluación de la función diastólica bajo la premisa de que el aumento crónico de presión AI conduce a la dilatación de la AI.
Se observa una reducción gradual del strain de reservorio a medida que empeora lafunción diastólica, y se descubrió que el strain de reservorio es el único parámetro de llenado del VI que se deterioró consistentemente a medida que empeoró la insuficiencia diastólica del VI, distinguiendo así todos los grados de función diastólica (Fig. 11).
-Parámetros suplementarios para valoración de la función diastólica.
1.- Duración de la onda transmitral A ( duración Ar-A)
La onda A transmitral y el flujo de la onda A venosa pulmonar (PVa) son causados por la contracción auricular y, por lo tanto, ocurren simultáneamente al final de la diástole. Cuando el VI es complaciente, la presión telediastolica es baja y ofrece baja resistencia a la contracción auricular, lo que da como resultado un mayor volumen de flujo que avanza hacia el VI que el flujo expulsado de regreso hacia los PV. Sin embargo, a pesar de las diferencias en volumen y velocidad, no hay diferencia en la duración entre el flujo A transmitral y PVa cuando la función diastólica es normal.
2.- Flujo de la vena pulmonar
El flujo fásico a través de las VP está gobernado por la relajación del VI, el compliance tanto del VI como de la AI y por la función de la AI. Como tal, los perfiles de flujo PV proporcionan información sobre el llenado del VI y la función diastólica. En ritmo sinusal, el flujo de VP se produce en tres fases (Fig. 12). Aunque los tiempos de desaceleración de las ondas PV S y PV D no son parámetros suplementarios dentro de los algoritmos diastólicos (se consideran medidas no rutinarias), se describen a continuación dentro de la descripción más amplia del flujo de las venas pulmonares.
Velocidad y desaceleración de la onda S en VP
La onda S puede tener dos picos identificables que corresponden a las dos fases del flujo durante este período: S1 y S2. Durante la sístole del VI e inmediatamente después de la contracción, el retroceso elástico de la AI hace que las dimensiones aumenten y la presión disminuya, lo que extrae un pequeño volumen de sangre de las PV hacia la AI por efecto de succión, identificado como onda S1. Durante la sístole media y tardía, el acortamiento continuo del VI y el descenso del anillo mitral hacia el ápex aumentan aún más las dimensiones de la AI, mientras que el SV del VD y la presión sistólica se propagan a través de los pulmones. La combinación de estos procesos impulsa una segunda onda S, identificada como S2. En general, debido a que el volumen de flujo VP generado por el retroceso de AI es mínimo, S2 es la contribución predominante a la velocidad máxima de la onda S (Fig. 12). En consecuencia, la velocidad de la onda S no sólo está influenciada por las propiedades diastólicas del VI y la presión de la AI, sino también por la contracción de la AI (que determina la magnitud del retroceso elástico), la relajación y distensibilidad de la AI, la distensibilidad del VI y la contractilidad del VI y del VD.
Velocidad y desaceleración de la onda D de venas pulmonares
La rápida relajación diastólica temprana del VI hace que la presión caiga por debajo de la presión de la AI, creando un efecto de succión que abre la VM y atrae sangre hacia el VI desde AI. A medida que la AI se vacía, la caída de presión de la AI hace que la sangre fluya desde las VP a través de la AI y hacia el VI, lo que se identifica como la onda D de PV (Fig. 12). La reducción de las dimensiones de la AI durante este período es secundaria a la relajación y el alargamiento del VI, empujando el anillo del VI hacia arriba y hacia el techo de la AI, sin ninguna contribución mecánica real por parte de la AI. Después de alcanzar su punto máximo en la diástole temprana, el flujo D de VP se desacelera gradualmente hasta el final del llenado diastólico temprano, lo que corresponde a la desaceleración del flujo transmitral. Como la velocidad y desaceleración de D reflejan el flujo directo de transmisión, éste se ve alterado por variaciones en la tasa de relajación del VI y en el presión AI.
Velocidad y duración de la onda Ar
Después de la fase temprana de llenado del VI, la contracción auricular al final de la diástole contribuye al resto del llenado total del VI. Sin embargo, si bien la distensibilidad normal del VI y la presión telediastolica normal/baja permiten que la mayor parte de la sangre expulsada por la AI ingrese al VI, un pequeño volumen de sangre se expulsa de regreso a las VP (Fig. 12). Por lo tanto, la velocidad y la duración del flujo retrógrado hacia las VP están determinadas por una serie de factores, que incluyen: precarga auricular, poscarga y función de bomba intrínseca de la AI. Cuando el función diastólica es normal, la duración del flujo retrógrado hacia los VP es igual o muy similar a la del flujo transmitral hacia el VI.
Relación PVS/PVD y fracción sistólica
Cuando la función diastólica es normal, la velocidad PV S suele ser igual o mayor que la velocidad PV D y, por lo tanto, la relación S/D suele ser >1; en atletas o personas jóvenes y en forma, la relajación rápida y altamente eficiente y el predominio del llenado temprano a menudo causan que la velocidad PV D exceda la velocidad PV S y una proporción de < 1. Disminución de la distensibilidad y función de bombeo de AI y aumento de presión de la AI secundario a una función diastólica deteriorada puede hacer que la velocidad de PV S1 caiga con la consiguiente reducción de la velocidad de PV S combinada, reduciendo así la relación PV S/D a < 1. La fracción sistólica de PV describe la relación de PV S y Flujo D y se puede calcular mediante PVS VTI/(PVS-VTI+PVDVTI). Una fracción sistólica <40% en aquellos con FEVI reducida proporciona una alta especificidad para presión AI elevada.
Desaceleración de la pendiente de la onda S de venas pulmonares (PV S)
La pendiente de desaceleración de la onda PV S se puede medir como un indicador del compliance de LA y, por lo tanto, de presión AI (Fig. 13).
Pendiente de desaceleración de la onda D de venas pulmonares.
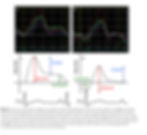
El llenado diastólico temprano del VI (onda E) y el flujo PV D ocurren simultáneamente. Debido a que la función AI no proporciona una contribución real al flujo de VP durante esta fase, los perfiles de flujo MV E y PV D están influenciados principalmente por la relajación del VI, mientras que el flujo PV D está influenciado adicionalmente por la distensibilidad de la AI y el aumento de la presión de la AI. La velocidad máxima del flujo de PV D aumenta a medida que aumenta LAP, mientras que la pendiente de desaceleración de la onda PV D (DTPVD) refleja la tasa de ecualización de presión entre AI y VI (Fig. 14) y, por lo tanto, la tasa de aumento de presión AI. Cuando se confirma una función diastólica alterada, un DTPVD más corto sugiere una presión AI elevado, mientras que un tiempo de desaceleración más largo sugiere un presion AI normal/bajo.
Velocidad y duración de PV Ar
El aumento de la presión diastólica del VI secundario a una disminución de la distensibilidad del VI aumenta la poscarga de la AI y la resistencia a la eyección de la AI. En consecuencia, el volumen, la velocidad y la duración del flujo transmitral directo procedente de la contracción auricular (VM A) disminuyen cuando se aumenta la presión diastolica del VI. Al mismo tiempo, debido a que la resistencia a la eyección de la AI es menor en las VP que en el VI, se expulsa un mayor volumen de sangre hacia las VP y durante un período más prolongado. Por lo tanto, la velocidad de PV Ar y la diferencia de duración entre MV A y PV Ar (duración de Ar-A) pueden considerarse indicadores de presiones diastólicas del VI elevadas, con una duración de Ar-A > 30 ms o una velocidad de PV Ar. >35 cm/s, lo que sugiere un aumento de la presión de la AI.
-Mediciones no rutinarias de la función diastólica.
Aunque los siguientes parámetros no se recomiendan para la práctica clínica habitual, pueden proporcionar información sobre la función diastólica en ciertos escenarios.
-Relación e´/a´
-TRIVI
-Velocidad de propagación
-Relación E/Vp
-TRIVI/Te-e´
-Tiempo de tránsito de la onda A
Algoritmo para la función sistolica normal.
Algoritmo para la función sistólica deteriorada.
Algoritmo para los pacientes en fibrilación auricular.
Hipertensión arterial pulmonar: diferenciando PH pre y poscapilar.
Conclusión
La evaluación de función diastolica es compleja y requiere un enfoque multiparamétrico para la investigación de la relajación, el compliance de la cámara y las presiones de llenado. Sin embargo, al considerar las recomendaciones contenidas en esta guía junto con la presentación clínica del paciente y, por lo tanto, identificar la probabilidad previa a la prueba de deterioro de la función diastólica, es posible realizar una investigación exitosa de la función diastólica y la presión telediastolica del VI en la mayoría de los pacientes.